 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
试用杂化轨道理论预测BF
试用杂化轨道理论预测BF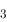 空间构型为 ,
空间构型为 ,
A.直线型
B.平面三角形
C.正四面体
D.三角锥形
提问人:网友lyle77
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
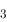 空间构型为 ,
空间构型为 ,A.直线型
B.平面三角形
C.正四面体
D.三角锥形
 更多“试用杂化轨道理论预测BF[图]空间构型为 ,A、直线型B、平…”相关的问题
更多“试用杂化轨道理论预测BF[图]空间构型为 ,A、直线型B、平…”相关的问题
根据杂化轨道理论,BF3分子的空间构型为______,NF3分子的空间构型为______。
根据杂化轨道理论预测下列分子的空间构型
PH3BBr3SiH4CO2HCN OF2H2O2
什么叫原子轨道的“杂化”?为什么要杂化?用杂化轨道理论解释为什么BF3的空间构型是平面三角,而NF3是三角锥形。
BF3分子是平面三角形的几何构型,NF3分子却是三角锥形的几何构型,试用杂化轨道理论加以说明。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题