 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由N2和H2化合生成NH3的反应中,[图]<0,当达到平衡后,再...
由N2和H2化合生成NH3的反应中,![由N2和H2化合生成NH3的反应中,[图]<0,当达到平衡后,再...由N2和H2化合生成NH3的反](http://static.jiandati.com/4ec4df0-chaoxing2016-446325.png) <0,当达到平衡后,再适当降低温度则平衡常数将________________。
<0,当达到平衡后,再适当降低温度则平衡常数将________________。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由N2和H2化合生成NH3的反应中,![由N2和H2化合生成NH3的反应中,[图]<0,当达到平衡后,再...由N2和H2化合生成NH3的反](http://static.jiandati.com/4ec4df0-chaoxing2016-446325.png) <0,当达到平衡后,再适当降低温度则平衡常数将________________。
<0,当达到平衡后,再适当降低温度则平衡常数将________________。
 更多“由N2和H2化合生成NH3的反应中,[图]<0,当达到平衡后…”相关的问题
更多“由N2和H2化合生成NH3的反应中,[图]<0,当达到平衡后…”相关的问题
计算题:合成氨的反应式为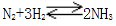 ,在400℃时,反应达到平衡,各物质的平衡浓度为:[N2]=3mol/L,[H2]=9=3mol/L,[NH3]=4mol/L。求在该温度下的平衡常数Kc、Kp以及N2和H2的原始浓度。
,在400℃时,反应达到平衡,各物质的平衡浓度为:[N2]=3mol/L,[H2]=9=3mol/L,[NH3]=4mol/L。求在该温度下的平衡常数Kc、Kp以及N2和H2的原始浓度。
A.H2和N2不再反应
B.H2、N2和NH3的浓度相等
C.NH3的浓度为零
D.H2、N2 的浓度为零
E.H2、N2和NH3的浓度不再变化
A.n(N2)减小、n(H2)减少、n(NH3)增大、Kθ不变
B. n(N2)减小、n(H2)减少、n(NH3)增大、Kθ增大
C. n(N2)、n(H2)、n(NH3)不变,Kθ不变
D. n(N2)增大、n(H2)增大、n(NH3)减小、Kθ不变
A.向正反应方向移动
B.向逆反应方向移动
C.状态不变
D.无法确定
A.n(N2)减小、n(H2)减少、n(NH3)增大、Kθ不变
B. n(N2)减小、n(H2)减少、n(NH3)增大、Kθ增大
C. n(N2)、n(H2)、n(NH3)不变,Kθ不变
D. n(N2)增大、n(H2)增大、n(NH3)减小、Kθ不变
A.c/(a+b-c)
B.c/(a+b+c)
C.c/(a+b+2c)
D.c/(a+3b+2c)
反应N3(g)+3H3(g)=2NH3(g)在一定温度下达平衡状态时,系统内n(N2)=4mol,n(H2)=n(NH3)=1mol。保持系统压力和温度恒定条件下,向系统中充入1mol氮气后,平衡如何移动?
反应N2(g)+3H2(g)→2NH3(g)的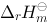 与反应N2(g)+H2(g)→NH3(g)的
与反应N2(g)+H2(g)→NH3(g)的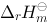 相同
相同
在1.0L容器中含有N2、H2和NH3的平衡混合物,其中有0.30mol N2,0.40molH2O,0.10mol NH3。如果温度保持不变,需向容器中加入多少摩尔的H2才能使NH3的平衡浓度增加一倍?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题