 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知TiO(OH)2的Ksp=4.0×10-30,TiO2+-OH-络合物的lgK1=14,求该沉淀在水中的溶解度。
已知TiO(OH)2的Ksp=4.0×10-30,TiO2+-OH-络合物的lgK1=14,求该沉淀在水中的溶解度。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知TiO(OH)2的Ksp=4.0×10-30,TiO2+-OH-络合物的lgK1=14,求该沉淀在水中的溶解度。
 更多“已知TiO(OH)2的Ksp=4.0×10-30,TiO2+…”相关的问题
更多“已知TiO(OH)2的Ksp=4.0×10-30,TiO2+…”相关的问题
A、0.0662 mol
B、0.124 mol
C、0.176 mol
D、0.353 mol
已知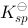 (AgCl) = 1.8×10
(AgCl) = 1.8×10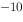 ,AgCl在0.001mol·L
,AgCl在0.001mol·L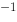 NaCl溶液中的溶解度为( )
NaCl溶液中的溶解度为( )
A、1.8×10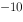 mol·L
mol·L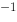
B、1.34×10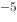 mol·L
mol·L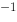
C、0.001mol·L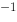
D、1.8×10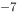 mol·L
mol·L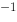
在pH=2.0的含有0.010mol·L-1EDTA及0.10mol·L-1HF溶液中,加入Ca2+,使Ca2+达0.10mol·L-1。问EDTA对CaF2沉淀生成有无影响?能否产生CaF2沉淀?[pKsp(CaF2)=10.57,pKa(HF)=3.18,lgK'CaY=10.69;pH=2.0时,lgαY(H)=13.51]
计算CaF2在pH=2.0,含Ca2+浓度为0.10mol·L-1溶液中的溶解度。(pKsp(CaF2)=10.57,HF的pKa=3.18)
在30.00mLAgNO3溶液中加入0.110%纯NaCl,过量的AgNO3需用3.50mL0.07100mol·L-1的KSCN溶液滴定至终点,计算AgNO3溶液的浓度。假设在上述滴定过程中未采取措施防止AgCl转化为AgSCN,则AgNO3溶液的实际浓度应为多少?相对误差有多大?(滴定至终点时溶液总体积为50.00mL,Ksp(AgCl)=1.8×10-10,Ksp(AgSCN)=1.0×10-12,M(NaCl)=58.44g·mol-1,[Fe3+]=0.015mol·L-1,滴定终点时,[(FeSCN)2+]=6.0×10-6mol·L-1,K(FeSCN2+)=138)
用MgNH4PO4重量法测定某磷矿样中P2O5的含量。称取含水分0.93%的该矿样0.6124g,经一系列处理后得到0.3425g Mg2P2O7。求分别以干基和以湿基计算时,矿样中P2O5的质量分数。[M(P2O5)=141.99g·mol-1,M(Mg2P2O7)=222.55g·mol-1]
某试样中约含50%的BaO,用BaSO4重量法测定其准确含量时,其中的Fe3+将共沉淀,若Fe3+共沉淀的量为溶液中。Fe3+含量的5%,那么要使Fe3+共沉淀引起的误差不大于0.1%,试样中Fe的含量应少于多少?[M(BaSO4)=233.39g·mol-1,M(Fe2O3)=159.69g·mol-1,M(BaO)=153.33g·mol-1,M(Fe)=55.847g·mol-1]


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题