 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
某一反应2A(g) = B(g)+E(g),反应物A消耗了2mol,此时的反应进度为()
A.-1mol
B.1mol
C.2mol
D.-2mol
提问人:网友xushiming
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.-1mol
B.1mol
C.2mol
D.-2mol
 更多“某一反应2A(g) = B(g)+E(g),反应物A消耗了2…”相关的问题
更多“某一反应2A(g) = B(g)+E(g),反应物A消耗了2…”相关的问题
(1)试结合图1.18.1所示的反应进程-势能图,定性判断该反应是吸热反应,还是放热反应,求算该反应的ΔtH;
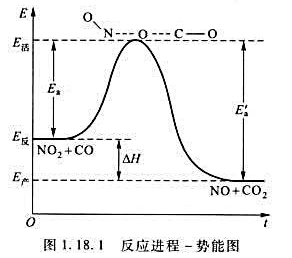
(2)若298K时的速率常数k=2.3×10-2s-1。试求373K时的速率常数;
(3)求算阿伦尼乌斯公式中的指前因子A。
A、-110.5kJ/mol
B、110.5kJ/mol
C、-676.5kJ/mol
D、676.5kJ/mol
A(g)=2B(g).已知平衡时nA=1.697mol,nB=4.606mol.
(1)求该温度下反应的Kθ和 ;
;
(2)若总压为50kPa,求平衡时A,B的物质的量.
A、|△G|增大,平衡常数减小
B、△H增大,反应速率减慢
C、反应历程改变,活化能增大,反应速率减小
D、|△G不变,平衡常数不变
反应2A+2B→2AB的速率方程为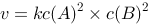 ,此反应()。
,此反应()。
A、一定是四级反应
B、一定是基元反应
C、一定是非基元反应
D、不能确定是否是基元反应


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题