 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
对于反应Sn(s)+2Cl2(g)=SnCl4(g),其标准摩尔反应焓变<0。在密闭容器中,反应达到平衡后,下列哪一个变化有利于增加sncl4的量(> A、升高温度
B、压缩体积
C、减少Cl2的量
D、加入氮气
提问人:网友jounys
发布时间:2022-01-07
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
B、压缩体积
C、减少Cl2的量
D、加入氮气
 更多“对于反应Sn(s)+2Cl2(g)=SnCl4(g),其标准…”相关的问题
更多“对于反应Sn(s)+2Cl2(g)=SnCl4(g),其标准…”相关的问题
A、HgS、SrS、FeS
B、CdS、FeS、CuS
C、CdS、HgS、CuS
D、CuS、SrS、CdS
已知E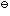 (Zn2+/Zn)= -0.763V,E
(Zn2+/Zn)= -0.763V,E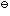 (Ni2+/Ni)= -0.25V。将下列反应:Zn(s)+Ni2+(aq)
(Ni2+/Ni)= -0.25V。将下列反应:Zn(s)+Ni2+(aq) Zn2+(aq)+Ni(s)构成一原电池,测得电动势为0.54V,且c(Ni2+)=1.0mol·L-1,则此时c(Zn2+)为()。
Zn2+(aq)+Ni(s)构成一原电池,测得电动势为0.54V,且c(Ni2+)=1.0mol·L-1,则此时c(Zn2+)为()。
A、0.020mol·L-1
B、0.320mol·L-1
C、0.500mol·L-1
D、0.12mol·L-1
A、a1>a2
B、a1=a2
C、a1<a2<br> D、a1和a2可以取任意值
A、(1)(2)
B、(2)(3)
C、(3)(4)
D、(1)(4)
A、该反应一定自发
B、该反应的标准平衡常数一定会随反应温度上升而减小
C、该反应的标准平衡常数一定会随反应温度上升而增大
D、该反应一定非自发
A、化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率
B、在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值
C、在同一化学反应中,其化学反应速率可以用反应物浓度的改变来表示,也可以用生成物浓度的改变来表示,其值可能相同,也可能不相同
D、化学反应速率的单位是g /L·s,也可以是kg/L·s


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题