 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0; 87.2 J/K/mol
B.30.77kJ; 0
C.27.84kJ; 8.3 J/K/mol
D.2.94kJ; -78.9 J/K/mol
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“苯的正常沸点为353K,摩尔气化焓DvapHm=30.77k…”相关的问题
更多“苯的正常沸点为353K,摩尔气化焓DvapHm=30.77k…”相关的问题
A.0; 87.2 J/K/mol
B.30.77kJ; 0
C.27.84kJ; 8.3 J/K/mol
D.2.94kJ; -78.9 J/K/mol
A.27.8kJ;8.3J/(mol•K)
B.30.77kJ;0
C.0;87.2 J/(mol•K)
D.2.94 kJ; -78.9 J/(mol•K)
苯在正常沸点353 K下的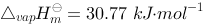 。今将353 K和标准压力下的1mol
。今将353 K和标准压力下的1mol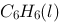 向真空等温汽化为同温、同压的苯蒸气(设为理想气体)。 (1)求算在此过程中苯吸收的热量Q与做的功W ; (2)求苯的摩尔汽化熵
向真空等温汽化为同温、同压的苯蒸气(设为理想气体)。 (1)求算在此过程中苯吸收的热量Q与做的功W ; (2)求苯的摩尔汽化熵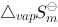 及摩尔汽化Gibbs自由能
及摩尔汽化Gibbs自由能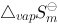 ; (3)求环境的熵变
; (3)求环境的熵变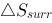 ; (4)应用有关原理判断上述过程是否为不可逆过程?
; (4)应用有关原理判断上述过程是否为不可逆过程?
已知苯在101.325kPa,80.1℃时沸腾,其气化潜热为30878J·mol-1。液态苯的Cp,m为142.7J·mol-1·K-1。将1mol、40.530kPa的苯蒸气在定温80.1℃下压缩至101.325kPa,然后凝结为液态苯,并将液态苯冷却到60℃,求整个过程的熵变。设苯蒸气为理想气体。
已知甲苯在正常沸点383K时的摩尔气化焓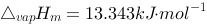 ,设气体为理想气体,凝聚态的体积与气体体积相比可忽略不计。 (1)1mol甲苯在正常沸点383K,可逆蒸发为同温、同压(101.325kPa)的蒸汽,计算该过程的Q,W,DU,DH,DS ,DA和DG; (2)如果是向真空蒸发变为同温、同压的蒸汽,计算该过程的Q,W,DU,DH,DS ,DA和DG; (3)请用熵判据,通过计算说明真空蒸发的可逆性和自发性。
,设气体为理想气体,凝聚态的体积与气体体积相比可忽略不计。 (1)1mol甲苯在正常沸点383K,可逆蒸发为同温、同压(101.325kPa)的蒸汽,计算该过程的Q,W,DU,DH,DS ,DA和DG; (2)如果是向真空蒸发变为同温、同压的蒸汽,计算该过程的Q,W,DU,DH,DS ,DA和DG; (3)请用熵判据,通过计算说明真空蒸发的可逆性和自发性。
已知苯(C6H6)在101.325kPa下于80.1℃沸腾,其△vapHm=30.878kJ·mol-1。液体苯的摩尔定压热容为Cp,m=142.7J·mol-1·K-1。今将40.53kPa,80.1℃的苯蒸气1mol,先恒温可逆压缩至101.325kPa,并凝结成液态苯,再在恒压下将其冷却至60℃。求整个过程的Q,W,△U,△H及△S。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题