 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于银锌电池:(-)Zn│Zn2+(1mol·L-1)‖Ag+(1mol·L-1)│Ag(),已知=-0.76V,=0.799V,该电池的标准电动势为()
A.1.180V
B. 0.076V
C. 0.038V
D. 1.559V
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1.180V
B. 0.076V
C. 0.038V
D. 1.559V
 更多“对于银锌电池:(-)Zn│Zn2+(1mol·L-1)‖Ag…”相关的问题
更多“对于银锌电池:(-)Zn│Zn2+(1mol·L-1)‖Ag…”相关的问题
(—)Zn|Zn。2+(1mol·L-1)||Ag+(1mol·L-1)|Ag()
A.增加Ag+的浓度
B.降低Ag+的浓度
C.增加Zn2+的浓度
D.加大锌极板
25℃,101 325 Pa的液态H2O的化学势为 (l),25℃,101 325 Pa的气态H2O的化学势为
(l),25℃,101 325 Pa的气态H2O的化学势为 (g) ,二者的关系是( )
(g) ,二者的关系是( )
A、 (l) >
(l) > (g)
(g)
B、 (l) <
(l) < (g)
(g)
C、 (l) =
(l) = (g)
(g)
D、无法判断
A、(-)Zn|Zn2+(1.0mol·L-1)║Cu|Cu2+(1.0mol·L-1)()
B、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1)|Fe2+(1.0mol·L-1)|Pt()
C、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1),Fe2+(1.0mol·L-1)()
D、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1),Fe2+(1.0mol·L-1)|Pt()
(1)Zn│ZnSO4(0.100mol/L)┊┊AgNO3(0.010mol/L)│Ag
(已知=-0.763V,=+0.80V)
(2)Pb│PbSO4(固),K2SO4(0.200mol/L)┊┊Pb(NO3)2(0.100mol/L)│Pb
(已知=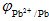 -0.126V,Ksp(PbSO4)=2.0×10-8)
-0.126V,Ksp(PbSO4)=2.0×10-8)
1.以Pt为电极,电解含有Ag+(0.01moldm-3)和Cu2+(1mol dm-3)的硫酸盐。假定[H+]=1mol dm-3,已知氢在铂电极上的超电势为0.4V,氧在铂电极上的超电势为0.5V,求在阴极析出物质的先后顺序及开始析出物质时对应的槽压。 已知φϴAg+/ Ag = 0.799 V,φϴCu2+/ Cu = 0.337 V。 2. 298K时,欲回收电镀液中的银,废液中AgNO3浓度为10-6mol·L-1 ,还含有少量的Cu2+存在,若以石墨为阴极,银用阴极电解法回收,要求回收99%的银.计算中令活度系数γ1 =1。试计算:(1) Cu2+的浓度应低于多少?(2)阴极电位应控制在什么范围内?(3)什么情况下Cu与Ag同时析出? 3. 以惰性电极电解SnCl2的水溶液进行阴极镀Sn,阳极中产生O2,已知:αSn2+ = 0.10 , αH+ =0.010,阳极上ηO2 =0.50V,已知:φϴSn2+/Sn = -0.140V,φϴH+,H2O/O2 = 1.23V, (1)试写出电极反应,并计算实际分解电压,(2)若 φH2,阴=0.40V,试问要使αSn2+ 降低到何值时才开始析出氢? 注意:以上题目均不考虑氧分压。
A、增加,增加
B、降低,降低
C、增加,降低
D、降低,增加
A、Sn^2+
B、MnO^4-
C、Sn^4+
D、PbO2


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题