 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“在络合滴定中,络合滴定剂EDTA具有哪些特点:”相关的问题
更多“在络合滴定中,络合滴定剂EDTA具有哪些特点:”相关的问题
A.αY(H), αY(N),αM(L)
B.αY(H), αY(N),αMY
C.αY(N), αM(L),αMY
D.αY(H),αM(L),αMY
A.在酸度高的溶液中,可能形成酸式络合物MHY
B.在碱度高的溶液中,可能形成碱式络合物MOHY
C.不论形成酸式络合物或碱式络合物均有利于络合滴定反应
D.不论溶液pH的大小,在任何情况下只形成MY一种形式的络合物
稀释至250nL容M瓶中,以水稀释到刻度并摇匀.准确移取50.00mL试液,以焦磷酸掩蔽其中的Fe3+和Cr3+,以紫脲酸铵作指示剂,需26.14mL0.05861mol·L-1EDTA溶液滴定至终点另一份50.00nL试液以六亚甲基四胺掩蔽其中的Cr3+,以紫脲酸铵作指示剂,需上述浓度的EDTA济液35.64mL滴定至终点:第三份50.00mL试液中加入50.00mL上述浓度的EDTA溶液,仍以紫脲酸铵作指示剂,需6.21mL0.06316mol·L-1Cu2+标准溶液返滴定至终点.计算此合金试样中Ni.Fe和Cr的质量分数.己知Ni.Fe、Cr的摩尔质量分别为58.69g.mol-1.55.847gmol-1和51.996gmol-1.
EDTA是化学分析中常用的一种()。
A.酸碱滴定剂
B.氧化还原滴定剂
C.沉淀滴定剂
D.络合滴定剂
Parda与其同事近期提出了一个间接测定自然界中(如海水、工业废水中)SO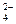 的方法。这方法是建立在:(1)让SO 生成PbSO4沉淀;(2)让PbSO4溶解在含有过量EDTA的氨溶液中,形成PbY2-络合物;(3)用Mg2+标准溶液滴定多余的EDTA。一些已知数据如下:
的方法。这方法是建立在:(1)让SO 生成PbSO4沉淀;(2)让PbSO4溶解在含有过量EDTA的氨溶液中,形成PbY2-络合物;(3)用Mg2+标准溶液滴定多余的EDTA。一些已知数据如下: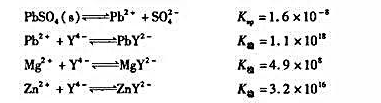
通过计算回答下列问题:
a.沉淀可否溶于含有Y4-的溶液?
b. Sporek提出了用Zn2+作滴定剂的类似方法,却发现结果的准确率很低,一种解释是Zn2+可能与PbY2-络合形成ZnY2-,用前面的平衡常数说明用Zn2+作滴定剂存在这个问题,而用Mg2作滴定剂却不存在这个问题的原因。Pb2+被Zn2+置换导致实验的结果偏高还是偏低?
c.在一次分析中,25.00ml的工业废水试样通过上述过程共消耗50.00ml 0.05000mol. L-1的EDTA。滴定多余的EDTA霜要12.24mL0.1000mol. L-1的Mg2+,试计算废水试样中SO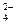 的浓度。
的浓度。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题