 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


已知2SO2 (g)+O2 (g)⇌2SO3 (g),起始时SO2和O别为20mol和10mol,达到平衡时SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为()
A.10mol 10%
B.20mol 20%
C.20mol 40%
D.30mol 80%
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


A.10mol 10%
B.20mol 20%
C.20mol 40%
D.30mol 80%
 更多“已知2SO2 (g)+O2 (g)⇌2SO3 (g),起始时…”相关的问题
更多“已知2SO2 (g)+O2 (g)⇌2SO3 (g),起始时…”相关的问题
试计算:
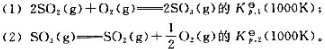
A.1/40
B.1/20
C.20
D.40
1000K,100kPa时,二氧化硫的氧化反应:
2SO2(g)+O2(g)====2SO3(g)
已知进料物质的量之比为SO2:O2=1:1,计算反应达平衡时系统的组成和SO2的转化率。1000K时SO2(g),O2(g),SO3(g)的标准摩尔生成吉布斯自由能函数值分别为:-329.3、0和-345.1kJ·mol-1。
在V2O5催化剂存在的条件下,已知反应: 2SO2(g)+O2(g)=2SO3(g) 在600℃和100kPa达到平衡时,SO2和O2的分压分别为10kPa和30kPa,如果保持温度不变,将反应体系的体积缩小到原来的一半,通过计算说明平衡移动的方向。
反应2SO2(g)+O2(g) 2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
2SO3(g)在1000K时的KƟ=3.4×10-5,计算1100K时的KƟ。已知该反应的ΔrHƟm=-189kJ/mol,并设在此温度范围内ΔrHƟm只为常数。
反应2SO2(g)+O2(g)=2SO3(g)在1000K时的KΘ=3.4×10-5,计算1100K时的KΘ。已知该反应的△rHmΘ=一189kJ/mol,并设在此温度范围内△rHmΘ为常数。
A.0.001mol/(L·min)
B.0.002mol/(L·min)
C.0.003mol/(L·min)
D.0.006mol/(L·min)
A.SO2、O2分别为0.4 mol·L-1、0.2 mol·L-1
B.SO2为0.25 mol·L-1
C.SO2、SO3均为0.15 mol·L-1
D.SO2为0.24 mol·L-1,SO3为0.14 mol·L-1
A.加入催化剂
B.移走SO3
C.升高温度
D.缩小容器体积


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题