 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算题:已知溶液中[OH-]的浓度为1×10-8M,计算溶液的PH值。
提问人:网友tangmanyun2019
发布时间:2022-01-06
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“计算题:已知溶液中[OH-]的浓度为1×10-8M,计算溶液…”相关的问题
更多“计算题:已知溶液中[OH-]的浓度为1×10-8M,计算溶液…”相关的问题
100mL浓度为0.10mol•L-1的AgNO3溶液,加入过量NH3•H2O后,稀释至200mL。若此溶液中游离NH3的浓度为1molL-1,求溶液中Ag+的浓度。(已知[Ag(NH3)2]¬的lg1=3.40,lg2=7.40)
A.有沉淀析出
B.无沉淀析出
C.为饱和溶液
D.无法确定
已知298.15 K时Mg(OH)2的溶度积为5.61x10-12。计算:
(1) Mg(OH)2在纯水中的溶解度(mol·L-1),Mg2+及OH- 的浓度;
(2) Mg(OH)2在0.01 mol·L-1NaOH溶液中的溶解度;
(3)Mg(OH)2在0.01mol·L-1MgCl2溶液中的溶解度。
A.在酸性或碱性稀溶液中,H+和OH-浓度的乘积总是一个常数为1³10-14
B. 在中性溶液里H+和OH-浓度相等为1³10-7
C. 在酸性溶液里没有OH-
D. 在碱性溶液中OH-浓度比H+大
已知:pKayΘ(HCOOH)=3.75,pKayΘ(HAc)=4.75,p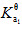 (H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
(H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题