 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在温度为T时,A(l)与B(l)的饱和蒸气压分别为30.0kPa和35.0kPa,当xA = 0.5时,pA = 10.0kPapB = 15.0kPa,则下列说法正确的是
A.该体系对拉乌尔定律产生正偏差
B.其T-x图上存在最高点
C.该体系能形成最低恒沸混合物
D.精馏时精馏塔底部可获得恒沸混合物
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.该体系对拉乌尔定律产生正偏差
B.其T-x图上存在最高点
C.该体系能形成最低恒沸混合物
D.精馏时精馏塔底部可获得恒沸混合物
 更多“在温度为T时,A(l)与B(l)的饱和蒸气压分别为30.0k…”相关的问题
更多“在温度为T时,A(l)与B(l)的饱和蒸气压分别为30.0k…”相关的问题
A、0.88
B、0.71
C、0.75
D、0.42
已知在20℃,H2O(l)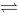 H2O(g),ΔrGmө=9.2kJ·mol-1,H2O(l)的饱和蒸气压为2.33kPa,则
H2O(g),ΔrGmө=9.2kJ·mol-1,H2O(l)的饱和蒸气压为2.33kPa,则
A、ΔrGmө>0,H2O(g)将全部变为液态
B、20℃,H2O(l)和H2O(g)不能达到平衡
C、20℃时,PH2O=2.33kPa,体系的ΔrGm=0
D、水蒸气压为100kPa时,平衡向形成H2O(g)的方向移动
A、0.2
B、0.4
C、0.6
D、0.8
某温度下xB=0.120的乙醇溶液蒸气压为101.325kPa,该温度下纯水的饱和蒸气压为91.326kPa,则亨利系数为
(A) 83.3kPa (B) 753kPa (C) 844kPa (D) 174.7kPa
(1)下面表示水的蒸气压与温度关系的方程式中的A和B值:
lgp=-A/T+B
(2)在此温度范围内水的摩尔蒸发焓;
(3)在多大压力下水的沸点为105℃。
液体H2O(A),CCl4(B)的饱和蒸气压与温度的关系如表6-4所示。
表6-4
|
两液体成完全不互溶系统。
(1)绘出H2O-CCl4系统气、液、液三相平衡时气相中H2O,CCl4的蒸气分压对温度的关系曲线;
(2)从图中找出系统在外压101.325kPa下的共沸点;
(3)某组成为yB(含CCl4的摩尔分数)的H2O-CCl4气体混合物在101.325kPa下恒压冷却到80℃时,开始凝结出液体水,求此混合气体的组成;
(4)上述气体混合物继续冷却至70℃时,气相组成如何?
(5)上述气体混合物冷却到什么温度度时,CCl4也凝结成液体,此时气相组成如何?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题