 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
以2×10-2mol/L EDTA滴定同浓度的Cd2+溶液,若pH为5.5,
以2×10-2mol/L EDTA滴定同浓度的Cd2+溶液,若pH为5.5,
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
以2×10-2mol/L EDTA滴定同浓度的Cd2+溶液,若pH为5.5,
 更多“以2×10-2mol/L EDTA滴定同浓度的Cd2+溶液,…”相关的问题
更多“以2×10-2mol/L EDTA滴定同浓度的Cd2+溶液,…”相关的问题
已知:pKayΘ(HCOOH)=3.75,pKayΘ(HAc)=4.75,p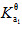 (H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
(H3PO4)=2.12;欲配制pH=3.5的缓冲溶液500mL,并使溶液中酸的浓度为0.20mol•L-1。应选用哪种缓冲对?需称取多少固体钠盐?
今欲配制pH=5.0、pCa=3.8的溶液,所需EDTA与Ca2+物质的量之比,即nEDTA:nCa为多少?[pH=5.0时,lgαY(H)=6.5;lgKCaY=10.7]
在pH=5.5时,0.01mol/L EDTA滴定0.01mol/LMg2+和0.01mol/L Zn2+混合溶液中的Zn2+,
在pH=5.00时,用2×10-4mol/L EDTA滴定同浓度的Pb2+,以二甲酚橙为指示剂,求ΔpM?
以铬黑T(EBT)为指示剂,在pH=10的NH3-NH4Cl缓冲溶液中,用0.02000mol/LEDTA滴定0.02000mol/L的Zn2+时,存在共存离子Ag+,其浓度是0.010mol/L。若在化学计量点时游离NH3的浓度为0.10mol/L:(1)能否准确滴定Zn2+? (2)计算该滴定的误差。
[lgKZnY=16.50;lgKAgY=7.32;pH=10时,lgKZn-EBT=12.2,lgαEBT(H)=1.6,lgαY(H)=0.45;Zn2+和Ag+的水解作用可忽略;银氨配合物的lgβ1=3.40、lgβ2=7.40;锌氨配合物的lgβ1=2.27、lgβ2=4.61、lgβ3=7.01、lgβ4=9.06]
在Al3+、Zn2+、Mg2+共存的酸性溶液中欲测定Mg2+,试指出以下分析步骤中的错误之处(简述理由),并改正。
吸取一定量试液于锥形瓶中,加入10%KCN 1mL,以NaOH溶液调节溶液的pH约等于10,加入1:3三乙醇胺15mL,再加入0.2%二甲酚橙指示剂2~3滴,以EDTA标准溶液滴至溶液由红紫变亮黄色为终点。
PAN在pH=2~12范围内呈黄色,它与Cu2+等金属离子的配合物显红色,但它与Ca2+不显色。为此,在pH=10~12时,加入适量的CuY,即可用PAN作为滴定Ca2+的指示剂,简述其原理。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题