 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时计算25℃时0.10mol·L-1H2S溶液中H3O-,HS-和S2+的
已知25℃时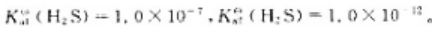 计算25℃时0.10mol·L-1H2S溶液中H3O-,HS-和S2+的浓度。
计算25℃时0.10mol·L-1H2S溶液中H3O-,HS-和S2+的浓度。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知25℃时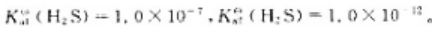 计算25℃时0.10mol·L-1H2S溶液中H3O-,HS-和S2+的浓度。
计算25℃时0.10mol·L-1H2S溶液中H3O-,HS-和S2+的浓度。
 更多“已知25℃时计算25℃时0.10mol·L-1H2S溶液中H…”相关的问题
更多“已知25℃时计算25℃时0.10mol·L-1H2S溶液中H…”相关的问题
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
一电导池充以0.02000mol·L-1的KCl溶液,25℃时测得其电阻为425Ω。已知25℃时0.02000mol·L-1KCl溶液的电导率为0.002768s·cm-1。在同一电导池中,装入同体积的浓度为0.555g·L-1的CaCl2溶液,测得电阻为850Ω。试计算:
计算25℃时,PbI2在水中的溶解度(mol.dm-3),已知PbI2的Kspθ=7.1×10-9。
25℃时,某种溶液中,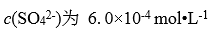 。若在 40.0L该溶液中,加入
。若在 40.0L该溶液中,加入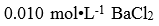 溶液 10.0 L,是否能生成BaSO4 沉淀?已知
溶液 10.0 L,是否能生成BaSO4 沉淀?已知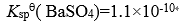
已知25℃时0.02mol·dm-3的KCl溶液的电导率为0.2768S·m-1。一电导池中充以此溶液,在25℃时测得其电阻为453Ω。在同一电导池中装入同样体积的质量浓度为0.555g·dm-3的CaCl2溶液,测得其电阻为1050Ω。计算:(1)电导池系数;(2)CaCl2溶液的电导率;(3)CaCl2溶液的摩尔电导率。
25℃时, 则25℃时AgSCN(s)在水中的溶解度s1=();在0.010mol·L-1AgNO3溶液中的溶解度s2=().
则25℃时AgSCN(s)在水中的溶解度s1=();在0.010mol·L-1AgNO3溶液中的溶解度s2=().


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题