 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由反应式 ,安排为电池 ,该电池的符号应是
,安排为电池 ,该电池的符号应是
A.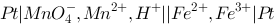
B.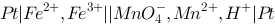
C.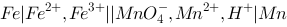
D.
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 ,安排为电池 ,该电池的符号应是
,安排为电池 ,该电池的符号应是A.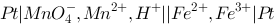
B.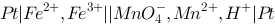
C.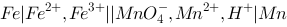
D.
 更多“由反应式 [图],安排为电池 ,该电池的符号应是A、[图]B…”相关的问题
更多“由反应式 [图],安排为电池 ,该电池的符号应是A、[图]B…”相关的问题
已知:锌电极 EΘ(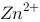 / Zn)=-0.763 v ,饱和甘汞电极EΘ=+0.242 v , ⑴ 写出由它们组成的原电池符号 ; ⑵ 写出正、负极反应式和电池反应式 ; ⑶ 计算该电池的电动势 EΘ、电池反应的 KΘ、∆ r GmΘ298 。
/ Zn)=-0.763 v ,饱和甘汞电极EΘ=+0.242 v , ⑴ 写出由它们组成的原电池符号 ; ⑵ 写出正、负极反应式和电池反应式 ; ⑶ 计算该电池的电动势 EΘ、电池反应的 KΘ、∆ r GmΘ298 。
已知:锌电极 EΘ(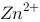 / Zn)=-0.763 v ,饱和甘汞电极EΘ=+0.242 v , ⑴ 写出由它们组成的原电池符号 ; ⑵ 写出正、负极反应式和电池反应式 ; ⑶ 计算该电池的电动势 EΘ、电池反应的 KΘ、∆ r GmΘ298 。
/ Zn)=-0.763 v ,饱和甘汞电极EΘ=+0.242 v , ⑴ 写出由它们组成的原电池符号 ; ⑵ 写出正、负极反应式和电池反应式 ; ⑶ 计算该电池的电动势 EΘ、电池反应的 KΘ、∆ r GmΘ298 。
原电池(-)Pt|Sn2+(c1),Sn4+(c2)||Sn2+(c3),Sn4+(c4)||Pt()负极反应式为______,正极反应式为______,此电池属于______电池,标准电池电动势为______V。
A、Zn为电池的负极
B、正极反应式为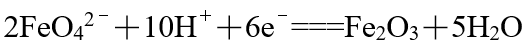
C、该电池放电过程中电解质溶液碱性增大
D、电池工作时OH-向负极迁移
某原电池的一个半电池是由金属银浸在1.0mol·dm-3Ag+溶液中组成的,另一半电池是由银片浸在c(Br-)为1.0mol·dm-3的AgBr饱和溶液中组成的。后者为负极。测得电池电动势为0.728V。试写出相关反应式。
试通过计算回答: (1)写出氢-氧燃料电池的电池总反应式。 (2)计算该电池的标准电动势(Eθ)。 (3)燃烧1mol氢气可获得的最大电功是多少?若该燃料电池的转化率为83.0%,则燃烧1mol氢气又可获得电功为多少(以千焦计)?


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题