 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。
已知![已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。已知 ,,试](https://img2.soutiyun.com/ask/2020-07-28/964777141030098.png) ,
,![已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。已知 ,,试](https://img2.soutiyun.com/ask/2020-07-28/96477714961559.png)
,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知![已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。已知 ,,试](https://img2.soutiyun.com/ask/2020-07-28/964777141030098.png) ,
,![已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。已知 ,,试](https://img2.soutiyun.com/ask/2020-07-28/96477714961559.png)
,试通过计算比较[Ag(NH3)2]+和[Ag(CN)2]+氧化能力的相对强弱。
 更多“已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN…”相关的问题
更多“已知 ,,试通过计算比较[Ag(NH3)2]+和[Ag(CN…”相关的问题
A、E^θ池=2E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
B、E^θ池=E^θ(Ag^+/Ag)]^2–E^θ(Zn^2+/Zn)
C、E^θ池=E^θ(Ag^+/Ag)–E^θ(Zn^2+/Zn)
D、E^θ池=E^θ(Zn^2+/Zn)–E^θ(Ag^+/Ag)
A、0.088mol·L-1;
B、0.27mol·L-1;
C、0.68mol·L-1;
D、0.29mol·L-1;
在0.1mol·dm-3的下列溶液中,c(Ag+)最大的是( )。
A.[Ag(S2O3)2]3-B.[Ag(NH3)2]+
C.[Ag(CN)2]-D.无法区分
A.[Ag(CN)2]-+2NH3====[Ag(NH3)2]++2CN-
B.[FeF6]3-+6SCN-====[Fe(SCN)6]3-+6F-
C.[Cu(NH3)4]2++Zn2+====[Zn(NH3)4]2++Cu2+
D.[HgCl4]2-+4I-====[HgI4]2-+4Cl-
A、5.9×10-9
B、8.9×10-9
C、4.6×10-9
D、7.3×10-9
比较AgCl在6mol·L-1氨水和水中的溶解度。已知KSP(AgCl)=1.8×10-10,KSP{[Ag(NH3)2]+}=1.12×107。
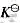 的值是()
的值是()A.由该反应的本质决定
B.由反应物和生成物的浓度决定
C.随反应物和生成物的浓度改变而改变
D.与系统是否处于标准状态有关


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题