 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知配离子[Zn(NH3)4]2+的磁矩为零,则其空间构型和成键时中心原子提供的杂化轨道分别为( )。
A.正四面体,sp3杂化
B.平面正方形,dsp2杂化
C.正八面体,d2sp3杂化
D.正八面体,sp3d2杂化
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.正四面体,sp3杂化
B.平面正方形,dsp2杂化
C.正八面体,d2sp3杂化
D.正八面体,sp3d2杂化
 更多“已知配离子[Zn(NH3)4]2+的磁矩为零,则其空间构型和…”相关的问题
更多“已知配离子[Zn(NH3)4]2+的磁矩为零,则其空间构型和…”相关的问题
(1)试通过下面NH3,N2H4,NH2OH碱式解离平衡常数,比较三者碱性大小并说明原因,
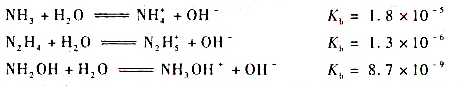
(2)举出反应实例说明硝酸的浓度对于其氧化性能和还原产物氧化态的影响。
(3)硝酸盐的热分解方式有哪几种?为什么会有这些分解方式?试各举一例说明。
(4)为什么NH3对于氢离子的配位能力比PH强,而PH3对于过渡金属离子的配位能力比NH3强?
(5)试说明P4O6与水的作用如何受温度的影响,P4O10与水的作用如何受水量的影响。
(6)磷的三种不同氧化数含氧酸H3PO4,H3PO3,H3PO2,为什么还原性随中心P原子的氧化数降低而增强?
(7)为什么NCI5及BrCl5不存在,而PCI5却可以?
(8)叠氮酸根负离子具有直线形结构,试分析其成键情况。
(9)试分析二氧化氮分子的成键情况,并找出实验根据。
(10)PO43-与Fe3+之间会发生什么反应?为什么说PO43-是Fe3+的掩蔽剂?
(11)画图表示链四聚和环四聚磷酸分子内原子间的键联关系,并写出链n聚和环n聚磷酸分子的通式。
(12)试用价层电子对互斥理论讨论PCI5和PBr5气态分子的构型。两者的晶体结构有什么特点?
(13)试说明马氏(Marsh)试砷法和古氏(Gutzeit)试砷法的原理和基本操作。
(14)As2O3,Sb2O3,Bi2O3的酸碱性有何规律?试通过具体化学反应加以说明。
(15)As2S3,Sb2S3,Bi2S3的酸碱性有何规律?试通过具体化学反应加以说明。
(1)试画出配位单元[CoCl2(NH3)4]+的几何异构体;
(2)实验测得此配位化合物的磁矩μ=0μB。试根据配位化合物的价键理论,画出中心钴离子的d电子在轨道中的排布示意图;
(3)写出中心钴离子在成键过程中所用的杂化轨道。
(1)O3;(2)NO3-;(3)AsI5;(4)NH3;(5)IF5;(6)POCl3;
| [化学—物质结构与性质] (1)依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 ①上述化学方程式中的5种物质所属的晶体类型有_________(填序号)。 a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体 ②基态铜原子的核外电子排布式为________。 (3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
①晶体Q中各种微粒间的作用力不涉及___________(填序号)。 a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力 ②R中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。 (4)已知苯酚( |
(1)中心原子A的价层电子对数为6,配体B的个数n=4;
(2)中心原子A的价层电子对数为5,配体B的个数n=2。
并利用得出的结论判断下列分子或离子的几何构型:
(3)I3-;(4)XeF2;(5)XeF4;(6)ICl4-。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题