 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“已知含铁(Fe2+)浓度为1.0mg/ml的溶液,用邻二氮菲…”相关的问题
更多“已知含铁(Fe2+)浓度为1.0mg/ml的溶液,用邻二氮菲…”相关的问题
计算在邻二氮菲存在下,溶液含H2S04浓度为1mol·L-1时,Fe3+/Fe2+电对的条件电势。(忽略离子强度的影响。已知在1mol·L-1H2S04中,亚铁络合物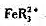 与高铁络合物
与高铁络合物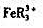 的稳定常数之比
的稳定常数之比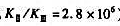 )
)
为分析硅酸盐中铁、铝、钛含量,称取试样0.6250g。除去SiO2后,用氨水沉淀铁、铝、钛为氢氧化物沉淀。沉淀灼烧为氧化物后重0.4165g。再将沉淀用K2S2O7熔融,浸取液定容于100mL容量瓶中。移取25.00mL试液通过锌汞还原器,含Fe2+和Ti3+的已还原液用含Fe3+的溶液承接,Fe3+被流入的Ti3+还原为Fe2+。然后用浓度为0.01390mol·L-1的K2Cr2O7标准溶液滴定,用去9.94mL。另取等量试液,用SnCl2将Fe3+还原为Fe2+,再用上述K2Cr2O7标准溶液滴定,用去8.82mL。计算试样中Fe2O3、Al2O3和TiO2的含量。[M(Fe2O3)=159.7g·mol-1,M(TiO2)=79.84g·mol-1,M(Al2O3)=102.0g·mol-1]
用邻二氮菲为显色剂测定铁,已知Fe2+的质量浓度为1.00×103μg·dm-3,比色皿的厚度为2cm,在508nm波长处测得吸光度为0.380,计算Fe2+的有色配合物在此波长处的摩尔吸收系数。
A.0.0005585
B.0.002792
C.0.005585
D.0.0027925
A、0.3351
B、0.5585
C、1.676
D、3.351

 如搜索结果不匹配,请
如搜索结果不匹配,请 


















