 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、共价键
B、范德华力
C、离子键
D、金属键
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“对同一元素而言,共价半径、金属半径和范德华半径相差不多。”相关的问题
更多“对同一元素而言,共价半径、金属半径和范德华半径相差不多。”相关的问题
如图,原先不带电的金属球壳的球心处放一点电荷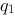 , 球外放一点电荷
, 球外放一点电荷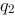
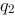 ,设
,设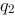 、金属内表面的电荷、外表面的电荷对
、金属内表面的电荷、外表面的电荷对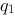 的作用力分别为
的作用力分别为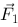 、
、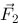 、
、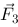 ,
,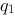 受的总电场力为
受的总电场力为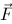 , 这几个力的大小分别用
, 这几个力的大小分别用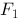 、
、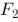 、
、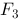 和
和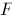 表示,则( )
表示,则( )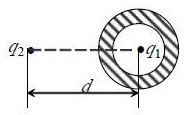
A、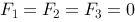
B、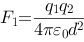 ,
,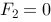 ,
,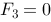 ,
,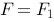
C、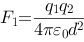 ,
,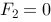 ,
,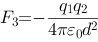 (即与
(即与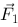 反向),
反向),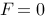
D、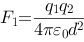 ,
,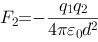 (即与
(即与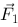 反向),
反向),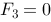 ,
,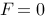
| [化学—物质结构与性质] (1)依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 ①上述化学方程式中的5种物质所属的晶体类型有_________(填序号)。 a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体 ②基态铜原子的核外电子排布式为________。 (3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
①晶体Q中各种微粒间的作用力不涉及___________(填序号)。 a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力 ②R中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。 (4)已知苯酚( |
B.Ⅰ A 族的卤化物均为离子键型
C.同一金属的不同氧化值离子形成卤化物时,高氧化值的金属离子形成的卤化物熔沸点较高
D.同一金属离子与不同的卤素离子形成卤化物时,随着卤素离子半径的增大,共价成分增多


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题