 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应的速率常数k=7.7×10-4s,又初始浓度为0.1mol·dm,则该反应的半衰期为()。 (A) 1443min (B) 15min (
某反应的速率常数k=7.7×10-4s,又初始浓度为0.1mol·dm,则该反应的半衰期为( )。
(A) 1443min (B) 15min (C) 30min (D) 217min
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某反应的速率常数k=7.7×10-4s,又初始浓度为0.1mol·dm,则该反应的半衰期为( )。
(A) 1443min (B) 15min (C) 30min (D) 217min
 更多“某反应的速率常数k=7.7×10-4s,又初始浓度为0.1m…”相关的问题
更多“某反应的速率常数k=7.7×10-4s,又初始浓度为0.1m…”相关的问题
某反应的速率常数k=5.0×10-5dm3·mol-1·S-1,若浓度单位改为mol·cm-3,时间单位改为min,则k的数值是
(A) 3 (B) 8.33×10-10(C) 8.33×10-4(D) 3×10-3
说明可逆反应的速率常数k+、k-与其平衡常数K之间关系。若已知某温度下氢氟酸的解离反应
HF(aq)====H+(aq)+F-(aq)
平衡常数为7.08×10-4mol·dm-3,又已知基元反应
H+(aq)+F-(aq)====HF(aq)
的速率常数为1.00×1011dm3·mol-1·s-1,试求氢氟酸解离反应的速率常数。
A.3.326(mol•dm-3)-1•s-1
B.3.0×10-4(mol•dm-3)-1•s-1
C.3326(mol•dm-3)-1•s-1
D.3.0×10-7(mol•dm-3)-1•s-1
将含有0.1mol·dm-3Na3AsO3和0.1mol·dm-3Na2S2O3的溶液与过量的稀硫酸溶液混合均匀,产生下列反应:
2H3AsO3(aq)+9H2S2O3(aq)→As2S3(s)+3SO2(g)+9H2O(l)+3H2S4O6(aq)
今由实验得在17℃时,从混合开始至溶液刚出现黄色的As2S3沉淀共需时1515s;若将上述溶液温度升高10℃,重复上述实验,测得需时500s,试求该反应的活化能Ea值。(提示:实验中,反应速率常用某物质一定浓度改变所需的时间来表示。)
298K时,在某一电导池中充以浓度为0.01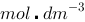 、电导率为0.14114
、电导率为0.14114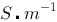 的KCl溶液,测得其电阻为525 Ω。若在该电导池内充以0.10
的KCl溶液,测得其电阻为525 Ω。若在该电导池内充以0.10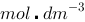 的
的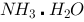 溶液时,测得电阻为2030 Ω,已知此时所用水的电导率为
溶液时,测得电阻为2030 Ω,已知此时所用水的电导率为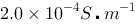 。试求: (1)该
。试求: (1)该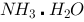 溶液的解离度; (2)若该电导池内充以纯水时的电阻值。
溶液的解离度; (2)若该电导池内充以纯水时的电阻值。
NO2二聚反应的速率方程为-dc(NO2)/dt=kc2(NO2),会使速率常数发生变化的条件是( )。
(A) 将体系的总压力加倍
(B) 在反应混合物中加O2
(C) 在反应混合物中加过量NO2
(D) 在CCl4溶液中进行反应而不在气相中反应
对反应2N2O5====4NO2+O2而言,当-dc(N2O5)/dt=0.25mol·dm-3·min-1时,dc(NO2)/dt的数值是( )。
(A) 0.06 (B) 0.13 (C) 0.50 (D) 0.25


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题