 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将下面的电池反应用电池行号表示:求电池:(1)标准电动势、标准自由能变以及反应平衡常数。(2)分别
将下面的电池反应用电池行号表示:
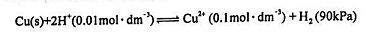
求电池:(1)标准电动势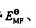 、标准自由能变
、标准自由能变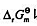 以及反应平衡常数。
以及反应平衡常数。
(2)分别根据EMF和 判断反应从左向右能否自发进行。
判断反应从左向右能否自发进行。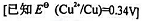
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将下面的电池反应用电池行号表示:
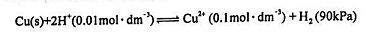
求电池:(1)标准电动势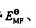 、标准自由能变
、标准自由能变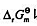 以及反应平衡常数。
以及反应平衡常数。
(2)分别根据EMF和 判断反应从左向右能否自发进行。
判断反应从左向右能否自发进行。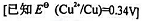
 更多“将下面的电池反应用电池行号表示:求电池:(1)标准电动势、标…”相关的问题
更多“将下面的电池反应用电池行号表示:求电池:(1)标准电动势、标…”相关的问题
标准状态下,由电对Ni2+/Ni和Pb2+/Pb组成电池。
(1)写出电池符号和电池反应方程式。
(2)计算电池电动势、电池反应的标准吉布斯自由能和平衡常数。
(3)在两电池溶液中同时加入S2-溶液,并使之都达到c(S2-)=1mol·L-1,求两电对的电极电势值,电池电动势和电池反应方向。
电池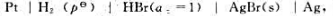 请:
请:
(1)写出电极反应与电池反应:
(2)若电池的电动势E/V=0.07131-4.99×10-6×(T/K-298),求正极在298K时的标准电极电势Eθ及电池反应的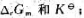
(3)判断此电池在298K时吸热还是放热,为什么?
(4)若HBr的浓度b=0.1mol·kg-1,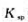 =1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
=1.00×10-12,电极Eθ(Ag+IAg)=0.80V,求电池的标准电动势Eθ.
A.标准摩尔反应吉布斯自由能和标准电动势都相同
B.标准摩尔反应吉布斯自由能相同,标准电动势不相同
C.标准摩尔反应吉布斯自由能不同,标准电动势相同
D.标准摩尔反应吉布斯自由能,标准电动势均不相同
298K时,电池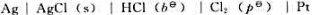 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数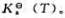
A.A.3X1.8/0.0592
B.B.6X1.8/0.0592
C.C.6X1.6/0.0592
D.D.3X1.6/0.0592
298K时,下列电池的电动势为1.228V:
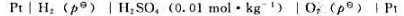
已知H2O(I)的标准生成焓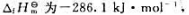 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
溶液适用Debye-Huckel极限公式.25℃时该电池电动势为0.5V.转移电子数为1时电池反应的摩尔反应焓为200kJ·mol-1,请:
(1)写出电极反应及电池反应;
(2)求25℃时,MCI的平均活度系数和电池的标准电动势:
(3)求此电池反应的ΔtGm、ΔtGmθ、ΔtSmθ和温度系数:
(4)求此电池在35℃时的电动势.
电池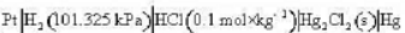 电动势召与温度T的关系为
电动势召与温度T的关系为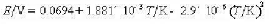
(1)写出电池反应:(2)计算25°C时该反应的DrCm.DrSm.DrHm以及电池恒温可逆放电时该反应过程的Qr.m


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题