 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在某温度下,0.1mol·dm-3氢氰酸(HCN)溶液的解离度为0.007%,试求在该温度时HCN的解离常数。
在某温度下,0.1mol·dm-3氢氰酸(HCN)溶液的解离度为0.007%,试求在该温度时HCN的解离常数。
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在某温度下,0.1mol·dm-3氢氰酸(HCN)溶液的解离度为0.007%,试求在该温度时HCN的解离常数。
 更多“在某温度下,0.1mol·dm-3氢氰酸(HCN)溶液的解离…”相关的问题
更多“在某温度下,0.1mol·dm-3氢氰酸(HCN)溶液的解离…”相关的问题
某温度下,反应N2(g)+3H2(g) 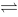 2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
A.正向进行
B.达到平衡状态
C.逆向进行
D.方向无法判断
A.150min
B.15min
C.30min
D.条件不够,不能求算
某温度下,反应N2(g)+3H2(g)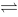 2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
A.正向进行
B.达到平衡状态
C.逆向进行
D.方向无法判断
某电导池装有0.1mol·dm-3的KCl水溶液,在25℃时测得电阻是28.65Ω,在同一电导池中换入0.1mol·dm-3的醋酸水溶液,测得电阻是703.0Ω。已知25℃时0.1mol·dm-3的KCl水溶液的电导率是1.289S·m-1。

298K时,在某半透膜的两边分别放入浓度为0.1mol·dm-3的大分子有机物RCl和浓度为0.5mol·dm-3的NaCl,设有机物RCl能全部解离,但R+不能透过半透膜。计算达到膜平衡后,两边各种离子的浓度和渗透压。
某电导池装有电导率为0.141S·m-1的KCI水溶液,在25℃时测得电阻是525Ω,在同一电导池中装入0.1mol·dm-3的NH3·H2O溶液,测得其电阻是2030Ω,计算NH3·H2O的解离度和标准解离平衡常数。
已知25℃下电池反应Cl2(100kPa)+Cd(s)====2Cl-(0.1mol·dm-3)+Cd2+(0.1mol·dm-3)
某电池(-)A|A2+(0.1mol·dm-3)||B2+(0.1mol·dm-3)|B()的电动势E为0.27V,则该电池的标准电动势为______。
(A) 0.24V (B) 0.27V (C) 0.30V (D) 0.33V


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题