 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某温度下,反应N2(g)+3H2(g)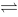 2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
A.正向进行
B.达到平衡状态
C.逆向进行
D.方向无法判断
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
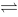 2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是
2NH3(g)的Kc = 0.56,若设法使CN2= 0.1mol·dm-3、CH2= 0.2 mol·dm-3、CNH3 = 0.05 mol·dm-3,按热力学角度则反应是A.正向进行
B.达到平衡状态
C.逆向进行
D.方向无法判断
 更多“某温度下,反应N2(g)+3H2(g)2NH3(g)的Kc …”相关的问题
更多“某温度下,反应N2(g)+3H2(g)2NH3(g)的Kc …”相关的问题
反应H2(g)+Br2(g)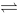 2HBr(g)的Kc=1.86。若将3mol H2,4mol Br2和5mol HBr放在10 dm3烧瓶中,则
2HBr(g)的Kc=1.86。若将3mol H2,4mol Br2和5mol HBr放在10 dm3烧瓶中,则
A、反应将向生成更多的HBr方向进行
B、反应向消耗H2的方向进行
C、反应已经达到平衡
D、反应向生成更多Br2的方向进行
A.Kp=Kc
B.KP=Kc×(RT)
C.Kp=Kc/(RT)
D.Kp=1/Kc
A、1.2×106
B、1.6×10-6
C、1.1×10-18
D、1.8×1024

A、必须低于 409.3℃
B、必须高于 409.3K
C、必须等于 409.3K
D、必须低于 409.3K

A、必须低于409.3℃
B、必须高于409.3 K
C、必须低于409.3K
D、必须等于409.3K
A、H2(g) + Cl2(g) === 2 HCl(g)
B、C(s) + 1/2 O2 (g) === CO(g)
C、CaCO3(s) === CaO(s) + CO2(g)
D、C(s) + O2(g) === CO2(g)
当反应2NO2(g)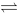 N2O4(g)达到平衡时,降低温度混合气体的颜色会变浅,说明此反应的逆反应是
N2O4(g)达到平衡时,降低温度混合气体的颜色会变浅,说明此反应的逆反应是
A、ΔrHmө=0的反应
B、ΔrHmө>0的反应
C、ΔrHmө<0的反应<br> D、气体体积减小的反应
反应A+B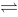 C,焓变小于零,若温度升高10℃,其结果是
C,焓变小于零,若温度升高10℃,其结果是
A、对反应没有影响
B、使平衡常数增大一倍
C、不改变反应速率
D、使平衡常数减小
对于反应2CO(g)+O2(g) 2CO2(g),ΔrHmө= -569 kJ·mol-1,提高CO的理论转化率的措施是
2CO2(g),ΔrHmө= -569 kJ·mol-1,提高CO的理论转化率的措施是
A、提高温度
B、使用催化剂
C、充惰性气体以提高总压力
D、增加O2的浓度
反应N2(g)+3H2(g)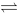 2NH3(g)ΔrHmө=-92kJ·mol-1,从热力学观点看要使H2达到最大转化率,反应的条件应该是
2NH3(g)ΔrHmө=-92kJ·mol-1,从热力学观点看要使H2达到最大转化率,反应的条件应该是
A、低温高压
B、低温低压
C、高温高压
D、高温低压


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题