 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
25℃时,试通过计算说明反应在25℃、标准状态下能正向自发进行。
25℃时,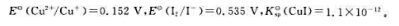 试通过计算说明反应
试通过计算说明反应
在25℃、标准状态下能正向自发进行。
提问人:网友18***469
发布时间:2022-05-30
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,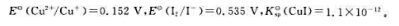 试通过计算说明反应
试通过计算说明反应
在25℃、标准状态下能正向自发进行。
 更多“25℃时,试通过计算说明反应在25℃、标准状态下能正向自发进…”相关的问题
更多“25℃时,试通过计算说明反应在25℃、标准状态下能正向自发进…”相关的问题
已知25°C时AgBr的溶度积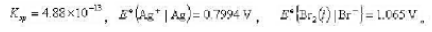 试计算25°C时
试计算25°C时
(1)银-溴化银电极的标准电极电势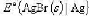 ;
;
(2)AgBr(s)的标准生成吉布斯函数。
反应 在35°C时二者皆增为2倍。试求:
在35°C时二者皆增为2倍。试求:
(1)25°C时的平衡常数。
(2)正、逆反应的活化能及反应热。
已知25°C时AgBr的活度积Kap=4.88x10-13,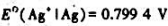 ,
,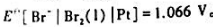 .试计算25℃时
.试计算25℃时
(1)银-溴化银电极的标准电极电势Eθ[Br-|AgBr(s)|Ag];
(2)AgBr(s)的标准摩尔生成吉布斯函数.
已知
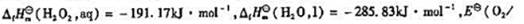
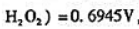
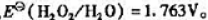
试计算25℃时反应2H2O2(I)→2H2O(l)+O2(g)的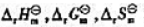 和标准平衡常数Kθ.
和标准平衡常数Kθ.
试利用标准热力学函数数据,通过计算回答汽车尾气净化反应:NO(g)+CO(g)=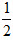 N2(g)+CO2(g)在25℃的标准条件下能否自发进行,并(用一句话)说明人们为此反应寻求高效催化剂有无现实意义。
N2(g)+CO2(g)在25℃的标准条件下能否自发进行,并(用一句话)说明人们为此反应寻求高效催化剂有无现实意义。
若已知25℃时Ni(OH)2饱和溶液的pH=9.20,试计算Ni(OH)2的标准溶度积常数为多少。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题