 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
应用德拜一休克尔极限公式计算25°C时0,002mol·kg-1CaCl2溶液中
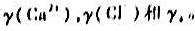
提问人:网友18***590
发布时间:2022-05-24
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
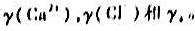
 更多“应用德拜一休克尔极限公式计算25°C时0,002mol·kg…”相关的问题
更多“应用德拜一休克尔极限公式计算25°C时0,002mol·kg…”相关的问题
应用德拜-休克尔公式计算25℃时下列各溶液中的γ±:
(1)0.005mol·kg-1NaBr;(2)0.001mol·kg-1ZnSO4。
德拜-休克尔极限公式适用于()
A.强电解质浓溶液
B.弱电解质浓溶液
C.强电解质稀溶液
D.弱电解质稀溶液
A.电解质的无限稀摩尔电导率Λ都可以由Λm与c1/2作图外推到c1/2 = 0得到
B.德拜—休克尔公式适用于强电解质
C.电解质溶液中各离子迁移数之和为1
D.若a(CaF2) = 0.5,则a(Ca2+) = 0.5,a(F-) = 1
A.稀溶液中强电解质完全电离
B.每一个离子都被相反电荷的离子氛所包围
C.每一个离子都是溶剂化的
D.离子间的静电引力导致电解质溶液偏离理想溶液的行为
A.溶液中导电的是离子而不是分子
B.任何浓度的强电解质都是完全电离的
C.离子之间以静电力相互作用, 其间的吸引能大于它们的热运动能
D.在稀溶液中离子是刚性的圆球形点电荷,不极化。


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题