 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将Cu片插入c(Cu2+)和C(Cl-)均为1.0 mol.L-1的溶液中,试计算Eθ(Cu2+/CuCl)和Eθ(CuCl/Cu),判断体系
将Cu片插入c(Cu2+)和C(Cl-)均为1.0 mol.L-1的溶液中,试计算Eθ(Cu2+/CuCl)和Eθ(CuCl/Cu),判断体系中可能发生什么反应?写出有关反应方程式。(已知Eθ(Cu2+/Cu+)=0.16 V,Eθ(Cu+/Cu)=0.52 V;Kspθ(CuCl)=1.2×10-6)
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
将Cu片插入c(Cu2+)和C(Cl-)均为1.0 mol.L-1的溶液中,试计算Eθ(Cu2+/CuCl)和Eθ(CuCl/Cu),判断体系中可能发生什么反应?写出有关反应方程式。(已知Eθ(Cu2+/Cu+)=0.16 V,Eθ(Cu+/Cu)=0.52 V;Kspθ(CuCl)=1.2×10-6)
 更多“将Cu片插入c(Cu2+)和C(Cl-)均为1.0 mol.…”相关的问题
更多“将Cu片插入c(Cu2+)和C(Cl-)均为1.0 mol.…”相关的问题
将Cu片插入c(Cu2+)和c(Cl-)均为1.0mol·L-1的溶液中,试计算




通过计算说明,将Cu片插入c(Cu2+)和c(Cl-)均为1.0mol·dm-3的溶液中,能否发生反应。若能发生反应写出反应方程式:
A.H2 + Cl2 ═ 2HCl
B.2Fe3+ + Cu ═ 2Fe2+ + Cu2+
C.g+ + Cl- ═ AgCl
D.2Hg2+ + SnCl2 ═ Hg2Cl2 + Sn4+
 值是( )
值是( )
A.-2.38V
B.-1.70V
C.-1.02V
D.+1.70V
 ,现把等物质的量的CuSO4、FeCl3和Zn置于水中,充分反应后,反应器中所得混合物除了SO
,现把等物质的量的CuSO4、FeCl3和Zn置于水中,充分反应后,反应器中所得混合物除了SO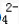 、Cl-外还有()。
、Cl-外还有()。
A.Zn2+、Cu、Fe2+
B. Zn2+、Cu2+、Fe、Fe2+
C. Zn2+、Cu2+、Fe2+
D. Zn2+、Cu2+、Cu、Fe2+
A.Fe2+和H2
B.Fe2+和Cu
C.Mg和H2
D.Fe2+和Cl2
A.Fe2+;
B.Cu
C.Mg
D.Cl-
将铜片插入含l.0 mol.L-1氨水和1.0 mol.L-1[Cu(NH3)4]2+的溶液中构成一个半电池,将此半电池与标准氢电极组成原电池,测得其电动势Eθ=0.030 V,且知标准氢电极在此作正极。试计算[Cu(NH3)4]2+的K稳θ。(已知:Eθ(Cu2+/Cu)=0.337 V)


为了保护您的账号安全,请在“简答题”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 简答题
简答题



 微信搜一搜
微信搜一搜
 简答题
简答题